Ароматические углеводороды (арены): классификация, номенклатура и изомерия, физические свойства. Физические и химические свойства аренов Арены структурная формула
ТЕМА 20. Ароматические углеводороды ряда бензола.
Гомологический ряд. Общая формула. Номенклатура. Изомерия.
Природные источники и методы получения: из алифатических, алициклических и ароматических соединений. Реакции Вюрца-Фиттига и Фриделя-Крафтса.
Физические свойства бензола и его гомологов.
Химические свойства. Реакции электрофильного замещения: галогенирование, нитрование, сульфирование, алкилирование и ацилирование. Реакции присое-динения водорода, галогенов, озона. Окисление бензола. Реакции гомологов бензола с участием боковой цепи: галогенирование, нитрование, окисление, дегидрирование.
Гомологический ряд. Общая формула.
Первым и наиболее важным представителем моноциклических ароматических углеводородов (аренов) является бензол С 6 Н 6 .
Отсюда общее название гомологического ряда ароматических углеводородов - ряд бензола.
Общая формула гомологического ряда бензола: С п Н 2п-6 .
Номенклатура аренов.
Для наименования аренов часто используются тривиальные названия: бензол, толуол, стирол, кумол и т.д.
По международной заместительной номенклатуре арены рассматриваются как производные бензола, в которых положение заместителей указывается цифрами, при этом номера атомов углеродов, у которых расположены заместители должны быть наименьшими:
метилбензол этилбензол изопропилбензол
(толуол) (кумол)

винилбензол этинилбензол
(стирол) (фенилацетилен)
В случае двух одинаковых заместителей вместо цифр можно пользоваться приставками: 1,2- (орто-), 1,3- (мета-), 1,4- (пара-):

1,2-диметилбензол 1,3-диметилбензол 1,4-диметилбензол
(орто-ксилол) (мета-ксилол) (пара-ксилол)
АРЕНЫ (ароматические углеводороды)
Арены или ароматические углеводороды – это соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Почему "Ароматические"? Т.к. некоторые из ряда веществ имеют приятный запах. Однако в настоящее время в понятие "ароматичность" вкладывается совершенно иной смысл.
Ароматичность молекулы означает ее повышенную устойчивость, обусловленную делокализацией π-электронов в циклической системе.
Критерии ароматичности аренов:
- Атомы углерода в sp 2 -гибридизованном состоянии образуют цикл.
- Атомы углерода располагаются в одной плоскости (цикл имеет плоское строение).
Замкнутая система сопряженных связей содержит
4n+2 π-электронов (n – целое число).
Этим критериям полностью соответствует молекула бензола С 6 Н 6 .
Понятие “бензольное кольцо ” требует расшифровки. Для этого необходимо рассмотреть строение молекулы бензола.
В
се связи между атомами углерода в бензоле одинаковые (нет как таковых двойных и одинарных) и имеют длину 0,139нм. Эта величина является промежуточной между длиной одинарной связи в алканах (0,154нм) и длиной двойной связи в алкенах (0,133 им).Равноценность связей принято изображать кружком внутри цикла
Круговое сопряжение дает выигрыш в энергии 150 кДж/моль. Эта величина составляет энергию сопряжения — количество энергии, которое нужно затратить, чтобы нарушить ароматическую систему бензола.
Общая фоормула: C n H 2n-6 (n ≥ 6)
Гомологический ряд:
Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы (R):
орто
- (о
-)
заместители у соседних атомов углерода кольца, т.е. 1,2-;
мета
- (м
-)
заместители через один атом углерода (1,3-);
пара
- (п
-)
заместители на противоположных сторонах кольца (1,4-).
арил
C 6 H 5 - (фенил ) и C 6 H
Ароматические одновалентные радикалы имеют общее название "арил ". Из них наиболее распространены в номенклатуре органических соединений два:C 6 H 5 - (фенил ) и C 6 H 5 CH 2 - (бензил ). 5 CH 2 - (бензил ).
Изомерия:
структурная:
1) положения заместителей для ди -, три - и тетра -замещенных бензолов (например, о -, м - и п -ксилолы);
2) углеродного скелета в боковой цепи, содержащей не менее 3-х атомов углерода:
3) изомерия заместителей R, начиная с R = С 2 Н 5 .
Химические свойства:
Для аренов более характерны реакции, идущие с сохранением ароматической системы , а именно, реакции замещения атомов водорода, связанных с циклом.
2. Нитрование
Бензол реагирует с нитрующей смесью (смесью концентрированныхазотной и серной кислот):
3. Алкилирование
Замещение атома водорода в бензольном кольце на алкильную группу(алкилирование ) происходит под действием алкилгалогенидов или алкенов в присутствии катализаторов AlCl 3 , AlBr 3 , FeCl 3 .
Замещение в алкилбензолах:
Гомологи бензола (алкилбензолы) более активно вступают в реакции замещения по сравнению с бензолом.
Например, при нитровании толуола С 6 Н 5 CH 3 может происходить замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола:
и облегчает замещение именно в этих положениях.С другой стороны, под влиянием бензольного кольца метильная группа СH 3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH 4 .
Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO 4 при нагревании):
Легче, чем в алканах, протекают реакции радикального замещения в боковой цепи алкилбензолов:
Это объясняется тем, что на лимитирующей стадии легко (при невысокой энергии активации) образуются устойчивые промежуточные радикалы. Например, в случае толуола образуется радикал бензил Ċ H 2 -C 6 H 5 . Он более стабилен, чем алкильные свободные радикалы (Ċ Н 3 , Ċ H 2 R), т.к. его неспаренный электрон делокализован за счет взаимодействия с π-электронной системой бензольного кольца:
Правила ориентации
- Заместители, имеющиеся в бензольном ядре, направляют вновь вступающую группу в определенные положения, т.е. оказывают ориентирующее действие.
По своему направляющему действию все заместители делятся на две группы: ориентанты первого рода и ориентанты второго рода .
Ориентанты 1-го рода (орто-пара -ориентанты) направляют последующее замещение преимущественно в орто - и пара -положения.
К ним относятся электронодонорные группы (электронные эффекты групп указаны в скобках):
R (+I ); - OH (+M,-I ); - OR (+M,-I ); - NH 2 (+M,-I ); - NR 2 (+M,-I ) +M-эффект в этих группах сильнее, чем -I-эффект.
Ориентанты 1-го рода повышают электронную плотность в бензольном кольце, особенно на углеродных атомах в орто - и пара -положениях, что благоприятствует взаимодействию с электрофильными реагентами именно этих атомов.Ориентанты 1-го рода, повышая электронную плотность в бензольном кольце, увеличивают его активность в реакциях электрофильного замещения по сравнению с незамещенным бензолом.
Особое место среди ориентантов 1-го рода занимают галогены, проявляющие электроноакцепторные свойства:
-F (+M<–I ), -Cl (+M<–I ), -Br (+M<–I ).
Являясь орто-пара
-ориентантами, они замедляют электрофильное замещение. Причина - сильный –I
-эффект электроотрицательных атомов галогенов, понижащий электронную плотность в кольце.
Ориентанты 2-го рода (мета
-ориентанты)
направляют последующее замещение преимущественно в мета
-положение.
К ним относятся электроноакцепторные
группы:
-NO 2 (–M, –I ); -COOH (–M, –I ); -CH=O (–M, –I ); -SO 3 H (–I ); -NH 3 + (–I ); -CCl 3 (–I ).
Ориентанты 2-го рода уменьшают электронную плотность в бензольном кольце, особенно в орто
- и пара
-положениях. Поэтому электрофил атакует атомы углерода не в этих положениях, а в мета
-положении, где электронная плотность несколько выше.
Пример:
Таким образом, легкость электрофильного замещения для соединений (приведенных в качестве примеров) уменьшается в ряду:
толуол C 6 H 5 CH В отличие от бензола его гомологи окисляются довольно легко.Определение, строение молекулы аренов.
Арены – это органические соединения, углеводороды карбоциклического ароматического характера, в молекулах которых имеется одно или несколько бензольных колец – циклических групп атомов углерода со специфическим характером связей бензольное ядро, и которые соответствуют общей формуле C n H 2 n -6 .
Бензол – простейший арен с молекулярной формулой С 6 Н 6 . Впервые формула была предложена А. Кекуле:
Строение молекул аренов.
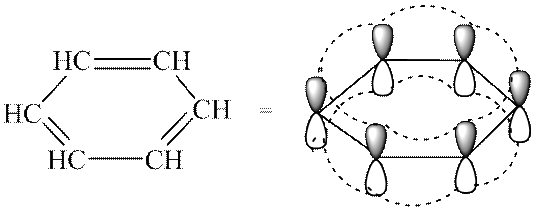
Все 6 атомов углерода находятся в sp 2 -гибридизации. Каждый атом углерода образует 2 σ -связи с двумя соседними атомами углерода и одним атомом водорода, которые находятся в одной плоскости. Углы составляют 120°. Т.е. все атомы углерода лежат в одной плоскости и образуют шестигранник. У каждого атома есть негибридная р -обиталь, на которой находится неспаренный электрон. Эта орбиталь перпендикулярна плоскости, и поэтому π -электронное облако «размазано» по всем атомам углерода:

Все связи равноценны. Энергия сопряжения – количество энергии, которую надо затратить, чтобы разрушить ароматическую систему.
Именно это обуславливает специфические свойства бензола – проявление ароматичности. Это явление было открыто Хюккелем, и называется правилом Хюккеля.
2. Изомерия аренов.
Арены можно разделить на 2 группы:
· производные бензола:

· конденсированные арены:

Общая формула аренов – С n H 2n-6 .
Для аренов характерна структурная изомерия, которая объясняется взаимным расположением заместителей в кольце. Если в кольце находится 2 заместителя, то они могут находиться в 3-х различных положениях – орто (о-), мета (м-), пара (п-).
А РЕНЫ
Ароматические углеводороды (арены) – циклические углеводороды, объединяемые понятием ароматичности, которая обуславливает общие признаки в строении и химических свойствах.
Классификация
По числу бензольных колец в молекуле арены подразделяются на:
моноядерные
многоядерные

Номенклатура и изомерия
Структурным родоначальником углеводородов бензольного ряда служит бензол С 6 Н 6 от которого строятся систематические названия гомологов.
Для моноциклических соединений сохраняются следующие несистематические (тривиальные) названия:

Положение заместителей указывают наименьшими цифрами (направление нумерации не имеет значения),
|
|
|
а для ди замещенных соединений можно использовать обозначения орто, мета , пара.
|
|
|
|
Если в кольце три заместителя тони должны получить наименьшие номера, т.е. ряд «1,2,4» имеет преимущество перед «1,3,4».


1,2-диметил-4-этилбензол (верное название) 3,4-диметил-1-этилбензол (неверно)
Изомерия монозамещенных аренов обусловлена строением углеродного скелета заместителя, у ди- и полизамещенных гомологов бензола добавляется ещё изомерия, вызванная различным расположением заместителей в ядре.
Изомерия ароматических УВ состава С 9 Н 12:
|
|
|
|
|
Физические свойства
Температуры кипения и плавления у аренов выше, чем у алканов, алкенов, алкинов, малополярные, не растворимы в воде и хорошо растворимы в неполярных органических растворителях. Арены это жидкости или твердые вещества, имеющие специфические запахи. Бензолы и многие конденсированные арены токсичны, некоторые из них проявляют концерогенные свойства. Промежуточными продуктами окисления конденсированных аренов в организме являются эпоксиды, которые либо сами непосредственно вызывают рак, либо являются предшественниками канцерогенов.
Получение аренов
Многие ароматические УВ имеют важное практическое значение и производятся в крупном промышленном масштабе. Ряд промышленных способов основан на переработке угля и нефти.
Нефть состоит главным образом из алифатических и алициклических УВ, для превращения алифатических или ациклических УВ в ароматические разработаны способы ароматизации нефти, химические основы которых развиты Н.Д. Зелинским, Б.А. Казанским.
1. Циклизация и дегидрирование:
2. Гидродезметилирование:

3. Гомологи бензола получают путем алкилирования или ацилирования с последующим восстановлением карбонильной группы.
а) Алкилирование по Фриделю-Крафтсу:

б) Ацилирование по Фриделю-Крафтсу:

4. Получение бифенила по реакции Вюрца-Фитинга:
5. Получение дифенилметана по реакции Фриделя-Крафтса:
Строение и химические свойства.
Критерии ароматичности:
На основании теоретических расчетов и экспериментального изучения циклических сопряженных систем было установлено, что соединение ароматично, если оно имеет:
- Плоский циклический σ-скелет;
- Сопряженную замкнутую π-электронную систему, охватывающую все атомы цикла и содержащую 4n + 2, где n = 0, 1, 2, 3 и т.д. Эта формулировка известна, как правило Хюккеля. Критерии ароматичности позволяют отличать сопряженные ароматические системы от всех других. Бензол содержит секстет π-электронов и соответствует правилу Хюккеля при n = 1.
Что дает ароматичность:
Несмотря на высокую степень ненасыщенности, ароматические соединения устойчивы к действию окислителей и температуры, они более склонны вступать в реакции замещения, а не присоединения. Эти соединения обладают повышенной термодинамической стабильностью, обеспечивающейся высокой энергией сопряжения ароматической системы кольца (150 кДж/моль), поэтому арены предпочтительней вступают в реакции замещения, в результате чего сохраняют ароматичность.
Механизм реакций электрофильного замещения в ароматическом кольце:
Электронная плотность π-сопряженной системы бензольного кольца является удобным объектом для атаки электрофильными реагентами.
Как правило, электрофильные реагенты генерируются в процессе реакции при помощи катализаторов и соответствующих условий.
Е – Y → E δ + – Y δ - → E + + Y -
Образование π-комплекса. Первоначальная атака электрофилом π-электронного облака кольца приводит к координации реагента с π-системой и образованию комплекса донорно-акцепторного типа называемого π-комплекса. Ароматическая система не нарушается:

Образование σ-комплекса. Лимитирующая стадия, на ней электрофил образует ковалентную связь с атомом углерода за счет двух электронов π-системы кольца, что сопровождается переходом данного атома углерода из sp 2 - в sp 3 - гибридное состояние и нарушением ароматической, молекула превращается в карбокатион.

Стабилизация σ-комплекса. Осуществляется путем отщепления от σ-комплекса протона с помощью основания. При этом за счет двух электронов разрывающейся ковалентной связи С – Н восстанавливается замкнутая π-системы кольца, т.е. происходит возврат молекулы в ароматическое состояние:

Влияние заместителей на реакционную способность и ориентацию электрофильного замещения
Заместители в бензольном кольце нарушают равномерность в распределении π- электронного облака кольца и тем самым оказывают влияние на реакционную способность кольца.
- Электронодонорные заместители (Д) повышают электронную плотность кольца и увеличивают скорость электрофильного замещения, такие заместители называют активирующими.
- Электроноакцепторные заместители (А) понижают электронную плотность кольца и уменьшают скорость реакции, называются дезактивирующими.
Бензол
Простейшим представителем аренов является бензол. Рассмотрим подробнее его свойства.
Физические свойства
Бензол представляет собой прозрачную бесцветную легколетучую жидкость с характерным запахом (именно по причине сильного запаха ароматические соединения получили свое название). Температура плавления 5,5°С, кипения - 80°С. Не смешивается с водой, но хорошо смешивается с большинством органических растворителей. Является растворителем для неполярных органических веществ. Горит коптящим пламенем (неполное сгорание) с образованием, кроме углекислого газа и воды, значительного количества сажи. Ядовит и как жидкость, и в виде паров при вдыхании.
Получение бензола
1. В промышленности бензол получают риформингом нефти, который по сути представляет собой дегидрогенизацию алканов нефти с образованием циклического скелета. В «чистом» виде основная реакция риформинга - это дегидрогенизация гексана:
Кроме того, бензол является одним из летучих продуктов коксования. Коксование - это нагревание каменного угля до 1000°С без доступа воздуха. При этом получается также много других ценных реагентов для органического синтеза и используемый в металлургии кокс. Также бензол можно получить тримеризацией ацетилена над активированным углем при 100°С.
2. В лаборатории бензол, разумеется, не получают, но теоретически методы его синтеза есть (они используются для получения его производных). И промышленные, и лабораторные методы отражены на приведенной ниже схеме.
Схема методов получения бензола
Промышленные методы.

Химические свойства бензола
Химические свойства бензола определяются, безусловно, его p-системой. Так же, как и в случае алкенов, она может быть атакована электрофильной частицей. Однако в случае ароматических соединений результат такой атаки будет совершенно иным. Высокая стабильность p-системы приводит к тому, что в конце реакции она, как правило, восстанавливается и результатом реакции является не присоединение (которое бы разрушило
p-систему), а электрофильное замещение. Рассмотрим подробнее его механизм.
На первой стадии атака молекулы АВ, содержащей электрофильный центр А, приводит к образованию крайне нестабильного p-комплекса (стадия 1). При этом ароматическая система не нарушена. Далее образуется ковалентная связь одного из атомов кольца с частицей А (стадия 2). При этом, во-первых, разрывается связь А-В, а во-вторых, разрушается p-система. Образовавшаяся нестабильная положительно заряженная молекула называется s-комплексом. Как уже было сказано, восстановление p-системы энергетически весьма выгодно, и это приводит к разрыву либо связи С-А (и тогда молекула возвращается в исходное состояние), либо связи С-Н (стадия 3). В последнем случае реакция заканчивается, и получается продукт замещения водорода на А.

Большинство реакций ароматических соединений имеют именно такой механизм (электрофильное замещение, сокращенно S E). Рассмотрим некоторые из них.
1. Галогенирование. Происходит только в присутствии катализаторов - кислот Льюиса (см. «Теория Льюиса»). Задача катализатора - поляризация молекулы галогена для образования хорошего электрофильного центра:
| АlСl 3 +Сl 2 «Сl + [АlСl 4 ] - Образовавшаяся частица имеет электрофильный атом хлора, и
происходит реакция:

К Нитрование. Осуществляется смесью азотной и серной кислот (нитрующей смесью). В нитрующей смеси происходит реакция:
HNO 3 +H 2 SO 4 «NO + 2 +Н 2 O
В образовавшемся гидросульфате нитрония есть мощный электрофильный центр - ион нитрония NO + 2 . Соответственно проходит реакция, общее уравнение которой:
![]()
3. Сульфирование. В концентрированной серной кислоте есть равновесие:
2H 2 SO 4 «SO 3 H + - +Н 2 O
В молекуле в правой части равновесия есть сильный электрофил SO 3 H + , который вступает в реакцию с бензолом. Результирующая реакция:
![]()
Алкилирование по Фриделю-Крафтсу. При взаимодействии бензола с алкилхлоридами или алкенами в присутствии кислот Льюиса (обычно галогенидов алюминия) получаются алкилзамещенные бензолы. В случае алкилгалогенидов первая стадия процесса:
RСl+АlСl 3 «R + [АlСl 4 ] - На второй стадии электрофильная частица R + атакует p-систему:
![]()
В случае алкенов кислота Льюиса поляризует двойную связь алкена, и на углероде опять-таки образуется электрофильный центр:

К неэлектрофильным реакциям относятся:
1. Гидрирование бензола. Эта реакция идет с разрушением p-системы и требует жестких условий (высокое давление, температура, катализатор - платиновые металлы):
![]()
2. Радикальное хлорирование. В отсутствие кислот Льюиса и при жестком ультрафиолетовом облучении бензол может реагировать с хлором по радикальному механизму. При этом разрушается p-система и образуется продукт присоединения хлора - твердое вещество гексахлоран, которое раньше использовалось в качестве инсектицида:

Гомологи бензола
Номенклатура и изомерия аренов
Все арены условно можно разделить на два ряда. Первый ряд - производные бензола (толуол, дифенил): второй ряд - конденсированные (полиядерные) арены (нафталин, антрацен).

Рассмотрим гомологический ряд бензола, соединения этого ряда имеют общую формулу С n Н 2 n . 6 . Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей в ядре. Монозамещенные производные бензола Не имеют изомеров положения, так как все атомы в бензольном ядре равноценны,
I Группа С 6 Н 5 называется фенильной. Фенильная и замещенные фенильные группы называются арильными. Ниже показаны некоторые производные бензола:
Схема реакций бензола


Изомеры с двумя заместителями в положениям 1,2; 1,3 и 1,4 называются орто-, мета- и пара-изомерами:

Номенклатура ароматических соединений
Ниже приведены названия некоторых ароматических соединений:
C 6 H 5 NH 3 + Сl - Фениламмоний хлорид (анилиний хлорид)
С б Н 5 СO 2 Н Бензолкарбоновая кислота (бензойная кислота)
C 6 H 5 CO 2 C 2 H 5 Этиловый эфир бензолкарбоновой кислоты (этилбензоат)
C 6 H 5 COCl Бензолкарбонилхлорид (бензоилхлорид)
C 6 H 5 CONH 2 Бензолкарбоксамид (бензамид)
C 6 H 5 CN Бензолкарбонитрил (бензонитрил)
C 6 H 5 CHO Бензолкарбальдегид (бензальдегид)
C 6 H 5 COCH 3 Ацетофенон
C 6 H 5 OH Фенол
C 6 H 5 NH 2 Фениламин (анилин)
C 6 H 5 OCH 3 Метоксибензол (анизол)
Эти названия соответствуют номенклатуре IUPAC. В скобках Указаны традиционные названия, которые по-прежнему широко распространены и вполне допустимы.
Номенклатура аренов
Название производного бензола с двумя или более заместителями в бензольном кольце строится таким образом. Атом углерода бензольного кольца, к которому присоединен заместитель, находящийся ближе других к началу приведенного выше списка, получает номер 1. Далее атомы углерода бензольного кольца нумеруются так, чтобы локант - номер второго заместителя - был наименьшим.
3-гидроксибензолкарбоновая кислота (3-гядроксибензойная кислота)
Карбоксильная группа рассматривается как главная группа, и ей присваивается локант «1». Нумерация кольца строится так, чтобы гидроксильная группа получила меньший («3», а не «5») локант.
2-аминобензолкарб альдегид (2-аминобензальдегид)
Группа -CHO рассматривается как главная. Она получает локант «1». Группа-NH 2 находится в положении «2», а не «6». Кроме того, допустимо название о-аминобензальдегид.
1-бром-2-нитро-4-хлорбензол Эти группы перечисляются в алфавитном порядке.
Получение аренов
Получение из алифатических углеводородов. При пропускании алканов с неразветвленной цепью, имеющих не менее 6 атомов углерода в молекуле, над нагретой платиной или оксидом хрома (III) происходит дегидроциклизация - образование арена с выделением водорода. Например:

2. Дегидрирование циклоалканов. Реакция происходит при пропускании паров циклогексана и его гомологов над нагретой платиной:
![]()
|. Получение бензола тримеризацией ацетилена. По способу Н. Д. Зелинского и Б. А. Казанского бензол можно получить, пропуская ацетилен через нагретую до 100°С трубку с активированным углем. Весь процесс можно изобразить схемой:

4. Получение гомологов бензола по реакции Фриделя-Крафтса (см. Химические свойства бензола).
5. Сплавливание солей ароматических кислот со щелочью: C 6 H 6 -COONa+NaOH ®C 6 H 6 +Na 2 CO 3
Применение аренов
Арены применяются как химическое сырье для производства лекарств, пластмасс, красителей, ядохимикатов и многих других органических веществ. Широко используют арены как растворители.
Реакции дегидрирования позволяют использовать углеводороды нефти для получения углеводородов ряда бензола. Они указывают на связь между различными группами углеводородов и на взаимное превращение их друг в друга.









